現在核酸医薬製造は大腸菌によるプラスミドDNAから製造することが標準となっています。
核酸医薬品市場は近年劇的に成長しており、先進的な治療法により重篤な疾患の治療に革新的な改善がもたらされています。
また、核酸医薬品は開発期間が短くて済むためモダリティとして注目が高まっています。
そこで弊社の大容量PCRシステムは、プラスミドDNA生産の手間とコストを下げ、かつ製造期間が短縮できるため、DNAに基づくあらゆる最先端の研究や治療分野での応用に適していると考えています。
大腸菌とPCRによるDNAの製造比較
━━
- pDNAよりも早く製造:大容量PCRは無細胞酵素製造プロセスを利用します。pDNAの場合に起こりえる製造の不安定性や数か月の日数は不要となります。理論上、数週間でDNA製造の可能性を秘めています。
- 不安定な配列:ITRやpolyA配列なども高い忠実度で増幅
- 細菌配列を排除:カルタヘナ法などの規制上の課題や薬剤耐性遺伝子を含む細菌由来の不要配列を排除可能。
- 大腸菌関連不純物は極力低減:無細胞製造プロセスのため、エンドトキシン、宿主タンパク質、大腸菌核酸などはほとんど混入しません。したがって、精製プロセスも簡素化されます。
- 拡張性:発酵ベースの生産よりも設置面積が大幅に小さい装置を使用して製造できます。
- 大規模なコストの削減:大容量PCRはDNAのコストが大幅に削減されます。
大腸菌とPCRによるDNAの製造比較
| 比較項目 | 大腸菌のプラスミドDNA | PCR DNA |
|---|---|---|
| DNA形状 | 環状 | 直鎖状 |
| DNAの収率 | 不安定 | 大腸菌の影響を受けない安定な収率 |
| 生産設備 | 大腸菌の培養、大腸菌集菌・溶菌、デプスフィルター設備 | 大容量PCR装置のみ |
| 製造期間 | 数日から数週間または数ヶ月 | 数時間から数日 |
| 大腸菌細胞精製工程 | 要 | 不要 |
| カルタヘナ法遵守 | 要 | 不要 |
| 正確性 | 約10-6 | 200ml PCR(3kb):約10-5 |
※次世代シークエンサーによる比較(弊社による)

mRNAの概要
インビトロトランスクリプション (IVT)による mRNA生成に最適なテンプレートです。弊社のプラットフォームは、マスターセルバンクを必要とせずに、迅速かつスケーラブルな開発を可能にし、同等の収量を得るために必要なDNA量を削減します。
サービス
初期テスト用の既製のレポーター遺伝子
IVT用の高純度DNAテンプレートのカスタム開発および製造
IVT 用のバルクDNAの線形化
迅速な応答プラットフォームのサポートとライブラリの生成
規制支援サービス

AAVの概要
一過性トランスフェクションによる AAV (アデノ随伴ウイルス) 産生においてプラスミド DNA をPCRで生産できます。
AAV 生産においてプラスミド DNA を酵素的に生成された PCR作製DNA に置き換えることにより、製造速度、安全性、拡張性が向上するとともに、複雑な配列や不安定な配列に関する多くの問題が解消されます。
サービス
repcap やヘルパー DNAなどの初期評価用の既製カタログ製品
目的のカスタム配列の DNAのmg を供給して実現可能性評価を実施します。これは、DNA プラットフォームで製品を評価するための迅速かつ簡単な方法です。
毒物学および cGMP材料の供給。お客様の規模とタイムラインに合わせた柔軟な供給と開発。

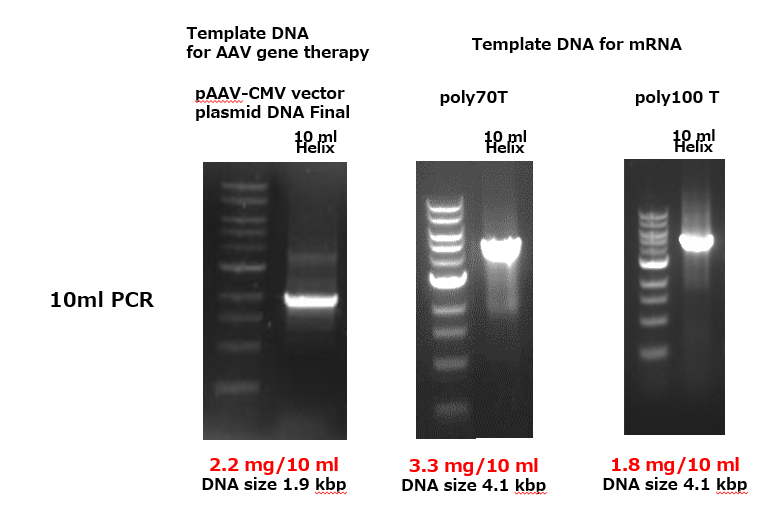
mRNA用polyA付加配列、AAV用ITR領域の増幅実績
その他
レンチウイルス、ゲノム編集、DNAワクチン、非ウイルス遺伝子治療等ご検討される場合は、先ずは弊社までご相談ください。



